viernes, 4 de diciembre de 2009
Sesión final de laboratorio (tema soluciones )
martes, 24 de noviembre de 2009
Libro una ojeada a la materia
La gran rapidez con que la ciencia y tecnología se han desarrollado en el mundo durante las últimas décadas ha tenido repercusiones sociales y culturales muy importantes....
El libro lo podras revisar en la siguiente dirección:
http://www.calidoscopio.com/calidoscopio/ecologia/quimica/materia.pdf
El Árbol Sintético
 http://www.cienciaynaturaleza.com.ar/PDF/eco12web%205.pdf
http://www.cienciaynaturaleza.com.ar/PDF/eco12web%205.pdfGeometría molecular
en:
http://www.ciencia-ahora.cl/Revista14/GeometriaMolecular.pdf
El Enlace Químico (III): moléculas poliatómicas

Geometría molecular: teoría RPECV Teoría RPECV: Teoría de la repulsión de los pares de electrones de la capa de valencia.... más, más, más en: http://www.upo.es/depa/webdex/quimfis/docencia/quimbiotec/curso0506/Tema7.pdf


FUERZAS INTERMOLECULARES
Visita: http://www.quimiweb.com.ar/sitio/2009/4.B-FUERZAS_INTERMOLECULARES.pdf
sábado, 14 de noviembre de 2009
ENLACE QUÍMICO
1. Contesta razonadamente ¿Cuál de los siguientes compuestos tendrá mayor punto de fusión:
fluoruro de sodio o bromuro de potasio?
(P.A.U. Jun. 96)
Rta.: NaF
2. ¿Cuál de los siguientes compuestos será más soluble en agua: yoduro de cesio u óxido de
calcio?
(P.A.U. Jun. 96 y Jun. 02)
Rta.: CsI
http://teleformacion.edu.aytolacoruna.es/ELVINAF2B8fb2/document/PAU_Quim_Es/PAUEnlaceEnunc.pdf
ENLACE QUÍMICO
2. Dadas las siguientes moléculas: fluoruro de oxígeno, yoduro de nitrógeno(III) y cloruro de azufre(II), indicar su geometría.
3. El trióxido de azufre y el ión nitrato presentan la misma geometría. Predecir esta geometría en base a la TRPECV y proponer la hibridación del átomo central.....
Más en:
http://www.educa.madrid.org/web/ies.cardenalcisnero.alcala/departamentos/webfq/docpdf/ej.enlace.pdf
viernes, 6 de noviembre de 2009
DETERMINACIÓN DE ENERGÍAS RETICULARES

Las energías reticulares ya calculadas, también pueden determinarse de los valores experimentales de los calores reacción y de cambio de fase de los participantes de una reacción química....
http://www.uc.cl/sw_educ/qda1106/CAP3/3A/3A3/index.htm
Enlace químico y estabilidad

Uniones entre átomos
Uno de los problemas más importantes de la química en el siglo XIX fue la justificación de las uniones entre los átomos. La teoría del enlace químico comenzó con el trabajo del químico alemán Richard Abegg (1869-1910) al explicar las uniones entre los átomos en términos de electrones; esta teoría da respuesta a preguntas como:
- ¿Por qué el oxígeno que respiramos, sustancia formada por moléculas constituidas por dos átomos de oxígeno, responde a la fórmula O2 y no a O?
- ¿Cómo se explica que el hidrógeno se una con el oxígeno para formar moléculas de agua (H2O)?
- Si sólo se dispone de un número reducido de elementos químicos, ¿por qué existe tal cantidad de sustancias diferentes?.....
Enlaces entre átomos
¿Por qué se unen los átomos?
visita
http://concurso.cnice.mec.es/cnice2005/93_iniciacion_interactiva_materia/curso/materiales/enlaces/enlaces1.htm
jueves, 5 de noviembre de 2009
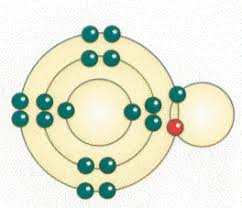
ENLACE QUÍMICO
¿POR QUÉ SE UNEN LOS ÁTOMOS?
Los átomos, moléculas e iones y se unen entre sí porque al hacerlo se llega a una situación de mínima energía , lo que equivale a decir de máxima estabilidad. Son los electrones más externos, los también llamados electrones de valencia los responsables de esta unión, al igual que de la estequiometría y geometría de las sustancias químicas.....
¿Cuánta energía es la mayor energía?
¿Qué es un electrón-voltio?
Es la energía que adquiere un electrón cuando es acelerado por una diferencia de potencial de un voltio....
más, más, más visita:
http://www.cienciahoy.org.ar/ln/hoy71/energia.htm
Propiedades periódicas de los elementos
La Tabla Periódica es una ordenación lógica y racional de todos los elementos químicos.
Hay diferentes versiones, las primeras se deben a D.I. Mendeleev y J.L. Meyer elaboradas en 1869; ambas estaban basadas en las repeticiones periódicas de las propiedades físicas y químicas de los elementos conocidos en aquella época. La versión moderna se basa en la configuración electrónica de los elementos químicos y se denomina “Forma Larga”....
http://www.ugr.es/~jruizs/Ficheros/EnlaceQ/Tema4.pdf
martes, 27 de octubre de 2009
El espín del electrón y el principio de exclusión de Pauli

http://www.hiru.com/es/fisika/fisika_06300.html
Evolución del modelo atómico actual
Tabla periódica
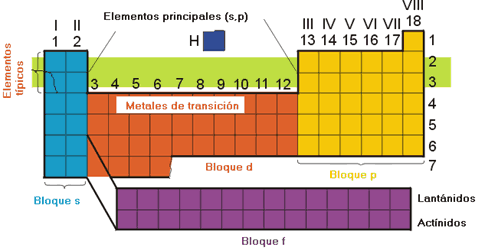
http://www.textoscientificos.com/quimica/inorganica/tabla-periodica
Tabla periódica
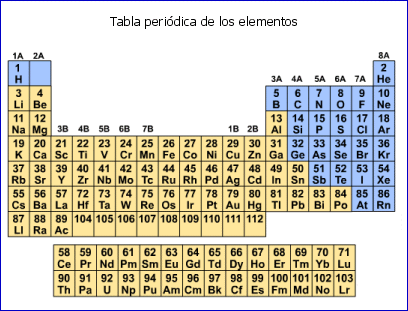
Únicamente ciertos electrones, llamados electrones de valencia, determinan las propiedades químicas de un elemento....
http://sel.uady.mx/ingenieria/courses/QBPROP/document/Parte_I/tablaperiodica.pdf?cidReq=QBPROP
jueves, 22 de octubre de 2009
EXCELENTE
PRACTIQUEN!!!!!
EL CEREBRO ES UN MÚSCULO MIENTRAS MÁS PRACTIQUEN MEJORES SERÁN
http://i.lumosity.com/
Guia de ejercicios química general

http://www.scribd.com/doc/7098854/Ejercicios-Quimica-General-Lo-de-4to-ano-Seria-Universidad-de-Andres-Bello
Visitala encontraras buenos ejercicios para practicar
Los nombres de los minerales

http://es.geocities.com/neolitos/mineralnames.html
Estructura de los cristales
 Sigueme:
Sigueme: http://www.xtal.iqfr.csic.es/Cristalografia/parte_01.html
Isótopos, número atómico y número másico

Los átomos están formados por un núcleo (formado por protones y neutrones), de tamaño reducido y cargado positivamente, rodeado por una nube de electrones, que se encuentran en la corteza.
El número de protones que existen en el núcleo, es igual al número de electrones que lo rodean. Este número es un entero, que se denomina número atómico y se designa por la letra, "Z".
continúa en http://www.eis.uva.es/~qgintro/atom/tutorial-05.html
martes, 13 de octubre de 2009
1er Parcial
http://docs.google.com/View?id=dcv6r36m_136df5w8pfh
sábado, 10 de octubre de 2009
Introducción a la Nomenclatura IUPAC de Compuestos Orgánicos
http://www.acienciasgalilei.com/qui/pdf-qui/iupac-form-organica.pdf
EJERCICIOS SOBRE LEYES PONDERALES
http://www.telefonica.net/web2/luissl/FisyQui1%BABach/u4leyesponderal.PDF
Ejercicios de repaso

Revisa http://www.scribd.com/doc/6629540/Ejercicios-de-Repaso-Ley-Proporciones-Definidas-y-Ley-de-Las-Proporciones-Multiples
Encontraras ejercicos para repasar.....
Premio Nobel de Química 2009
 El Premio Nobel de Química 2009 número 101 ha sido público hoy por la Fundación Nobel, y nuevamente son tres científicos quienes se repartirán el premio. Venkatraman Ramakrishnan, Thomas Steitz y Ada Yonath son los encargados de recibir el premio de US$1.4 millones gracias a su trabajo en investigación en los ribosomas.....
El Premio Nobel de Química 2009 número 101 ha sido público hoy por la Fundación Nobel, y nuevamente son tres científicos quienes se repartirán el premio. Venkatraman Ramakrishnan, Thomas Steitz y Ada Yonath son los encargados de recibir el premio de US$1.4 millones gracias a su trabajo en investigación en los ribosomas.....http://www.ojocientifico.com/2009/10/07/premio-nobel-de-quimica-2009/
Cristalografía
 Estas páginas pretenden guiar al lector interesado en el fascinante mundo de la Cristalografía, una parte del saber bien entroncada en la Ciencia actual y gracias a la cual hemos podido averiguar, a través del esfuerzo de muchas personas y durante muchos años, cómo son los cristales, cómo son las moléculas, las hormonas, los ácidos nucléicos, los enzimas, las proteínas ..., a qué se deben sus propiedades y cómo podemos entender su funcionamiento en una reacción química, en un tubo de ensayo, o en el interior de un ser vivo.....
Estas páginas pretenden guiar al lector interesado en el fascinante mundo de la Cristalografía, una parte del saber bien entroncada en la Ciencia actual y gracias a la cual hemos podido averiguar, a través del esfuerzo de muchas personas y durante muchos años, cómo son los cristales, cómo son las moléculas, las hormonas, los ácidos nucléicos, los enzimas, las proteínas ..., a qué se deben sus propiedades y cómo podemos entender su funcionamiento en una reacción química, en un tubo de ensayo, o en el interior de un ser vivo.....http://www.xtal.iqfr.csic.es/Cristalografia/
lunes, 5 de octubre de 2009
ejercicio
Encontraras el ejercicio que comenzamos en clase
jueves, 1 de octubre de 2009
Prueba corta 2. Semestre 2009-2
http://docs.google.com/View?id=dgz9fc3m_303dvx3cndj
Bienvenida a los nuevos estudiantes
 Creo en la ucv
Creo en la ucv creadora de ciencia y
de cultura, la de Vargas,
la del hombre justo
y bueno que sueña un país decente.
multicolores del pensamiento,
en su aula magna,
acaso el recinto

más hermoso y democrático
de la cultura nacional
y el único lugar
donde puede oírse
el silencio reflexivo de la multitud.
que dormitan tras
las nubes de Cl
 ader;
ader; en la dignidad del alma
ucevista y en los
nombres olvidados
de los que la hicieron
y la hacen grande.
de la docencia y la
cultura, puesto que
puede buscar el bien.
que mantienen viva
Mecenas de la lectura.
en la reproducción
clandestina de libros
y las ediciones piratas.
como el único mal negocio
que se justifica.
investigador solitario,
mal remunerado
y peor valorado,
en el estudiante que
marcha con su veinte
bajo el brazo.
como derecho irrenunciable
y en la obligación moral
que tiene la mayoría de
oponerse a una minoría
corrupta que ni la respeta
ni la representa.
y en la irreductible fuerza
del bien, en la pluma
Earle Herrera y en el arte
que se por los rincones insospechados
de la UCV.
cuya sola existencia es
suficiente para justificar
la universidad.
dicha que florece a la sombra
de las hojas azules del reloj,
ya que allí descubrí el amor.
Laureano Márquez
lunes, 28 de septiembre de 2009
Pureza de los reactivos
Cuando se realizan cálculos estequeométricos es necesario tener el cuenta el porcentaje de impurezas que tienen los reactivos.
http://quimicaparatodos.blogcindario.com/2009/09/00075-pureza-de-los-reactivos.html
martes, 22 de septiembre de 2009
NOMENCLATURA INORGANICA
Nomenclatura sistemática
Nomenclatura Stock
Nomenclatura tradicional
lunes, 21 de septiembre de 2009
Resultados primera prueba corta
http://docs.google.com/View?id=dgz9fc3m_302g3zv89d8
Reactivo limitante y rendimiento

http://www.eis.uva.es/~qgintro/esteq/tutorial-04.html
Nomenclatura Química

http://www.cespro.com/Materias/MatContenidos/Contquimica/QUIMICA_INORGANICA/nomenclatura_qca.htm
viernes, 18 de septiembre de 2009
Grupos de laboratorio
En: http://docs.google.com/View?id=dgz9fc3m_300gsk5k9rc
podras saberlo....

miércoles, 16 de septiembre de 2009
Para practica
http://www.lapaginadejc.com.ar/Quimica.htm
En este enlace web encontraras apuntes de temas, ejercicios y otros materiales excelentes para estudiar

Utilizan desechos para producir energía limpia
Metanol como combustible
Metanol como combustible
En principio cabe destacar que el metanol surge como combustible alternativo ante la toxicidad de las emisiones de las naftas y la destrucción de la capa de ozono....Visita: http://www.textoscientificos.com/quimica/metanol/metanol-como-combustible
martes, 15 de septiembre de 2009
CulturaGeneral.net
http://www.culturageneral.net/Ciencias/Quimica/Compuestos_Quimicos/
lunes, 14 de septiembre de 2009
Concepto de mol. Número de Avogadro

En el siguiente enlace http://www.hiru.com/es/kimika/kimika_01000.html
encontraras mas información al respecto
Nomenclatura

Visita: http://wapedia.mobi/es/Alfred_Stock
¿Exceso de números? Aprende a redondear al número correcto de cifras significativas
jueves, 10 de septiembre de 2009
Clase de práctica
Nombrar y formular un compuesto (BOOK "Nomenclature of Inorganic Chemistry - IUPAC Recommendations 2005")

La versión en castellano de nomenclatura inorgánica, titulada “Nomenclatura de Química Inorgánica Recomendaciones de la IUPAC de 2005”, recoge toda la información sobre el tema y existen libros de Química Inorgánica(asignatura que cursarás mas adelante) que tienen información al respecto que te ayudarán a la estudiante a alcanzar la capacidad de poder nombrar y formular muchas otras especies similares y le servirán en su proceso de aprendizaje y en su futuro profesional.
http://stage.iupac.org/objID/
Por ahora , en Química General I deberás conocer que existen diversos sistemas (Stock, sistematica, tradicional) de nomenclatura para los compuestos inorgánicos.
lunes, 7 de septiembre de 2009
IMPORTANTE PRACTICAS
Listado de estudiantes sección G1 y G2
 Quieres revisar en que sección quedaste visita:
Quieres revisar en que sección quedaste visita:http://spreadsheets.google.com/pub?key=t7rR_TwDhnykuGCEzzEE34g&output=html
http://spreadsheets.google.com/pub?key=th96Xu5LHV-3_tIEmzaFY5w&output=html
Programa semestre II-2009
 En la siguiente pagina:
En la siguiente pagina:http://docs.google.com/View?id=dgz9fc3m_274c72s3nfv
encontraras el programa para química general actualizado











